Trang chủ Thư viện
GIỚI THIỆU
Vào năm 2018, Dược điển Hoa Kỳ (USP) trong các Chương Tổng quát 1 và 2 đã cập nhật danh sách các nguyên tố và giá trị liều lượng tối đa cho phép hàng ngày (PDE) của tạp chất nguyên tố trong thuốc, các chất dược phẩm và nguyên liệu thô. USP hiện phù hợp với Hội đồng Quốc tế về Hài hòa Hóa (ICH) Q3D (R2) Bước 5, phiên bản mới nhất được thông qua vào năm 2022.
Chương này quy định danh sách các nguyên tố và giá trị liều dùng tối đa cho phép hàng ngày (PDE) theo các đường đưa thuốc vào cơ thể như: uống, tiêm (tiêm tĩnh mạch) và hít. Chương cũng nêu rõ quy trình chuẩn bị mẫu, quy trình phân tích và các quy trình kiểm soát chất lượng xác nhận đối với phân tích các nguyên tố được liệt kê trong chương. Hướng dẫn ICH Q3D (R2) Bước 5 áp dụng cho cùng nhóm sản phẩm dược phẩm và các chất dược phẩm, nhưng bổ sung thêm giới hạn cho các tạp chất nguyên tố khi sử dụng qua đường da và xuyên da. Đây là quy trình kiểm tra dựa trên rủi ro để đánh giá sự hiện diện tiềm ẩn của các nguyên tố độc hại.
USP khuyến nghị tính thích nghi của cả công nghệ ICP-OES và ICP-MS để phân tích tạp chất. Tuy nhiên, việc lựa chọn công nghệ phụ thuộc vào liều lượng tối đa cho phép hàng ngày (PDE), dạng liều lượng và số lượng liều hàng ngày. ICP-OES có độ nhạy và phạm vi động học tuyến tính để xử lý một số sản phẩm thuốc đường uống; tuy nhiên, để đạt được giới hạn phát hiện thấp nhất và phạm vi hiệu chuẩn rộng nhất, ICP-MS là kỹ thuật lý tưởng.
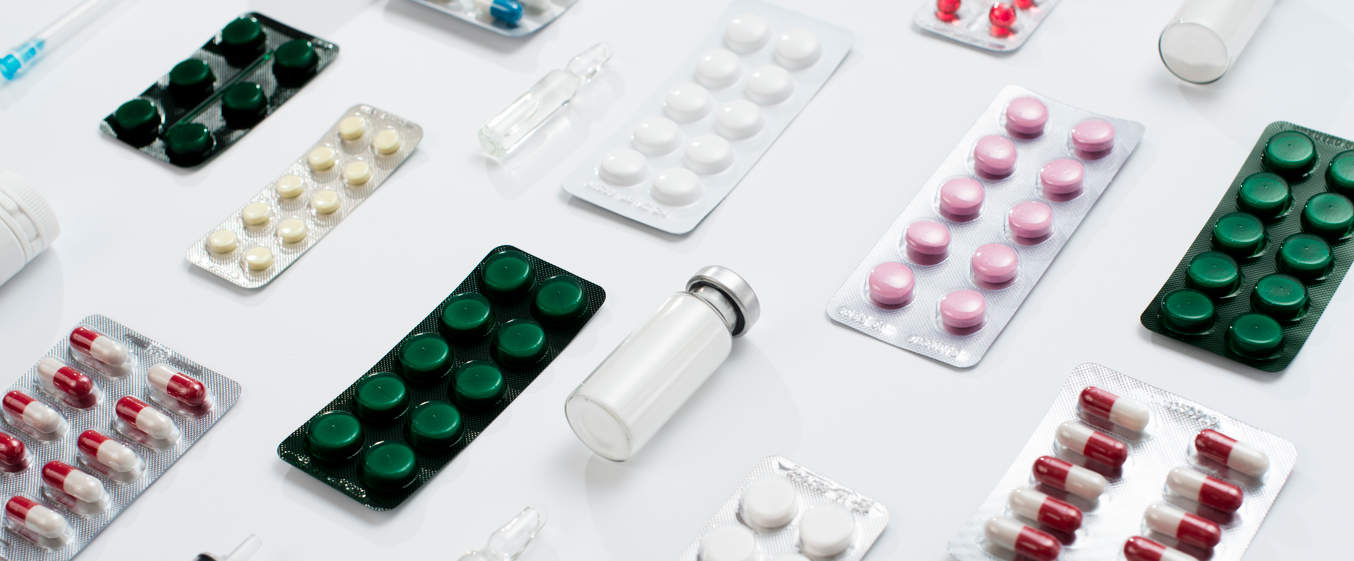
Trong Bảng 1, các nguyên tố được quy định và giới hạn PDE từ ICH Q3D được hiển thị theo các đường dùng thuốc. Chúng được chia thành ba loại (1, 2A/2B và 3), dựa trên độc tính và khả năng xuất hiện trong các sản phẩm thuốc. Ví dụ, các nguyên tố Loại 1 và 2A ít nhất phải được bao gồm trong đánh giá rủi ro ở tất cả các loại sản phẩm thuốc.
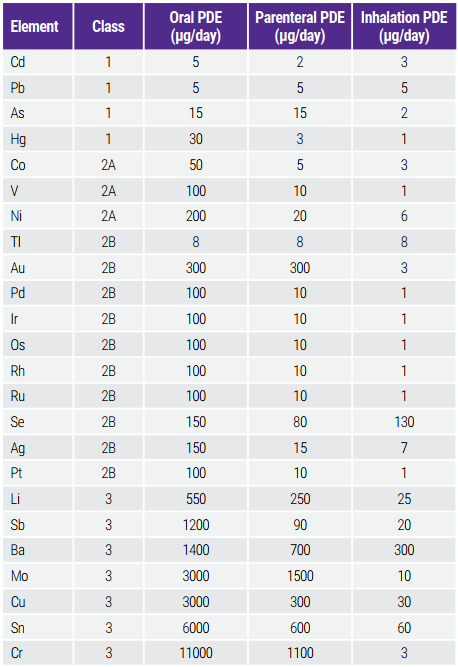
Bảng 1: Harmonized List of Elements and Established PDEs for Elemental Impurities
Khi giá trị PDE được biểu thị bằng µg/ngày chuyển đổi thành µg/g hoặc µg/L dựa trên liều dùng tối đa hàng ngày, chúng được gọi là Giới hạn Mục tiêu hoặc Nồng độ cho phép. Sau khi tính đến yếu tố pha loãng, chúng trở thành giá trị J, được tính như sau:
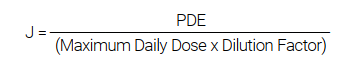
PerkinElmer cung cấp bộ kit USP/ICH, bao gồm cả máy tính J để tính toán chính xác giá trị J của tạp chất nguyên tố, giúp việc chuẩn bị tiêu chuẩn và phát triển phương pháp dễ dàng hơn. Nghiên cứu này tập trung vào lợi ích thực tiễn của NexION® 1100 ICP-MS cho việc xác định một nhóm các nguyên tố liên quan đến độc tố trong một lượng lớn dung dịch tiêm truyền tĩnh mạch (LVP) dược phẩm. Nó đưa ra tổng quan về phương pháp USP, với sự nhấn mạnh đặc biệt vào mức độ tạp chất và các quy trình phân tích được khuyến nghị. Các tiêu chí xác định hiệu suất của hệ thống dựa trên quy trình xác nhận USP cho phương pháp cũng được trình bày.
Thí nghiệm
Chuẩn bị mẫu
Dung dịch NaCl có độ tinh khiết cao (seaBlank, 10-11% NaCl, Elemental Scientific Inc., Omaha, Nebraska, USA) được sử dụng để chuẩn bị các dung dịch LVP (Large Volume Parenteral – Dung dịch tiêm truyền khối lượng lớn) mô phỏng (0,9% NaCl) bằng cách pha loãng 11 lần vào một dung dịch chứa 2% HNO3 và 2% HCl. Dung dịch LVP mô phỏng sau đó được pha loãng thêm 2 lần với dung dịch 2% HNO3 và 2% HCl, đạt nồng độ mặn cuối cùng là 0,45% trước khi phân tích. USP yêu cầu hiệu chuẩn thiết bị dựa trên tối thiểu hai tiêu chuẩn (0,5J và 1,5J). Các công ty dược phẩm thường sử dụng 0,3J như một phần của đánh giá rủi ro. Trong những trường hợp đặc biệt, nếu mẫu chứa một lượng bằng với giá trị J, các mẫu thêm vào 1,5J sẽ dẫn đến nồng độ là 2,5J. Nồng độ tiêu chuẩn hiệu chuẩn được hiển thị trong Bảng 2.
Các tiêu chuẩn hiệu chuẩn được chuẩn bị bằng cách pha loãng các tiêu chuẩn đa nguyên tố và đơn nguyên tố thương mại (xem bảng Vật tư tiêu thụ sử dụng) với nồng độ dựa trên PDEs, hệ số pha loãng là 2, và liều lượng hàng ngày của các mẫu dung dịch muối là 2 L/ngày. Tiêu chuẩn nội bộ bao gồm Ge 1000 ppb, Tb 20 ppb, và Bi 20 ppb trong dung dịch chứa 2% HNO3 và 2% HCl, được trộn trực tuyến với các mẫu trống, tiêu chuẩn và mẫu.
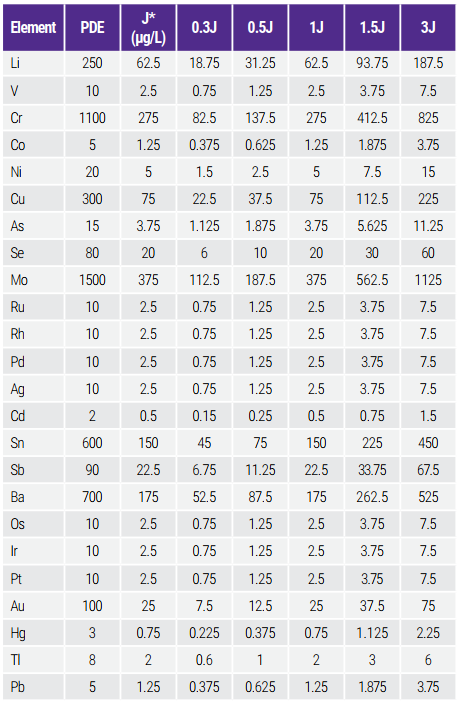
Bảng 2. PDEs (µg/day) and Calibration Standard Concentrations (µg/L) for LVP Saline Solution
Dụng cụ
Máy NexION 1100 ICP-MS (PerkinElmer, Shelton, Connecticut, USA) được sử dụng để phân tích các mẫu dung dịch muối LVP theo Chương của USP và ICH Q3D. NexION với thiết kế quang học ion được cấp bằng sáng chế — sự kết hợp giữa giao diện hình nón ba tầng và bộ làm lệch ion tứ cực — kết hợp sự đơn giản và tiện lợi của một buồng va chạm truyền thống với giới hạn phát hiện xuất sắc. Trong ứng dụng này, heli được sử dụng làm khí va chạm để đo tất cả các nguyên tố bằng chế độ va chạm (KED).
Các dòng khí buồng phản ứng được tối ưu hóa để đạt được các giới hạn phát hiện tốt nhất theo hướng dẫn vận hành của thiết bị. Một thông số mặc định RPq (tham số loại bỏ buồng phản ứng) được sử dụng cho tất cả các chất phân tích để đơn giản hóa quá trình phát triển phương pháp. Các nguyên tố, đồng vị của chúng, và các dòng khí heli (He) được sử dụng cho phân tích được liệt kê trong Bảng 3.
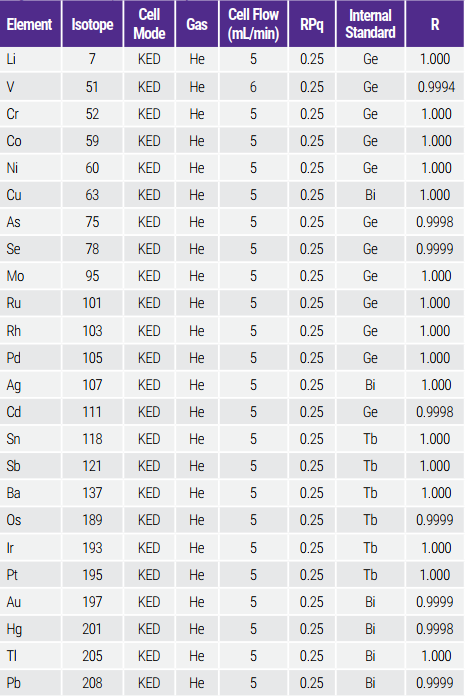
Bảng 3. Method Setup and Linearity
Dung dịch All Matrix Solution (AMS) với dòng khí Argon được đưa vào cổ buồng phun, thường được sử dụng cho các mẫu có tổng lượng chất rắn hòa tan (TDS) cao, được áp dụng ở đây để ổn định tín hiệu, và cung cấp thêm một bước pha loãng gấp hai lần.
Các thông số vận hành thiết bị được hiển thị trong Bảng 4. Trong chế độ va chạm (KED), tỷ lệ 35Cl16O/59Co thường là 0,5%. Đối với phân tích V của mẫu dung dịch muối LVP, tỷ lệ 35Cl16O+ /59Co+ cần được điều chỉnh xuống dưới 0,3%. Các cone mới được làm sạch cần được điều chỉnh trước khi phân tích mẫu. Trong phương pháp này, các cone được điều chỉnh bằng cách hút 0,45% NaCl trong 2% HNO3 và 2% HCl và theo dõi các nội chuẩn cho đến khi tín hiệu ổn định. Hệ thống sau đó được rửa bằng cách hút nước siêu tinh khiết, sau đó là dung dịch 2% HNO3 và 2% HCl trước khi bắt đầu các lần chạy mẫu.
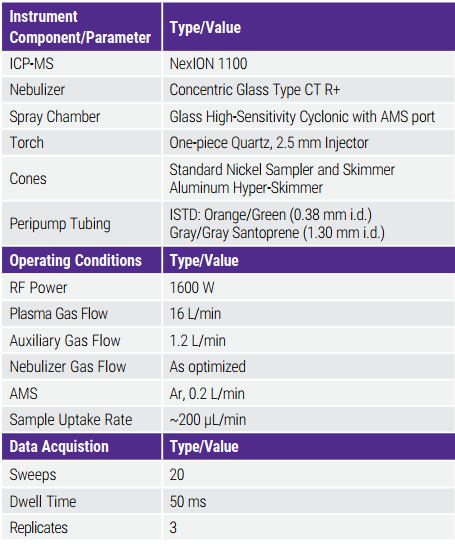
Bảng 4. Instrumental Parameters for LVP Saline Solution
Kết quả
USP <730>7 và <233> các tài liệu hướng dẫn định nghĩa một số quy trình QA/QC để kiểm tra và xác nhận trong việc phát triển phương pháp. Chúng bao gồm:
- Tính tuyến tính (Linearity)
- Giới hạn phát hiện (Limits of detection – Detectability)
- Độ phù hợp của hệ thống (System suitability – Stability)
- Độ chính xác (Accuracy)
- Độ chính xác lặp lại (Precision – Repeatability)
Tính tuyến tính (Linearity)
Tiêu chí xác nhận của hệ số tương quan cần lớn hơn 0,995 đối với các thử nghiệm Loại I và lớn hơn 0,99 đối với các thử nghiệm định lượng Loại II. Bảng 3 cho thấy các hệ số tương quan cao hơn 0,999 đã đạt được cho tất cả các chất phân tích trong các phạm vi hiệu chuẩn.
Giới hạn phát hiện (Limits of Detection)
Các giá trị của giới hạn phát hiện phương pháp (MDLs) và giới hạn định lượng phương pháp (MQLs) đã được thiết lập cho tất cả các nguyên tố trong nghiên cứu này để đảm bảo rằng khả năng phát hiện của phương pháp thấp hơn đáng kể so với mức giới hạn tạp chất nguyên tố tối đa (1.0J). MDL được tính bằng cách nhân 3 với độ lệch chuẩn (SD) của ba lần đo mẫu natri clorua 0,45% có độ tinh khiết cao (n=7) và MQL là 10*SD của ba lần đo mẫu natri clorua 0,45% tinh khiết cao. Kết quả được hiển thị trong Bảng 5.
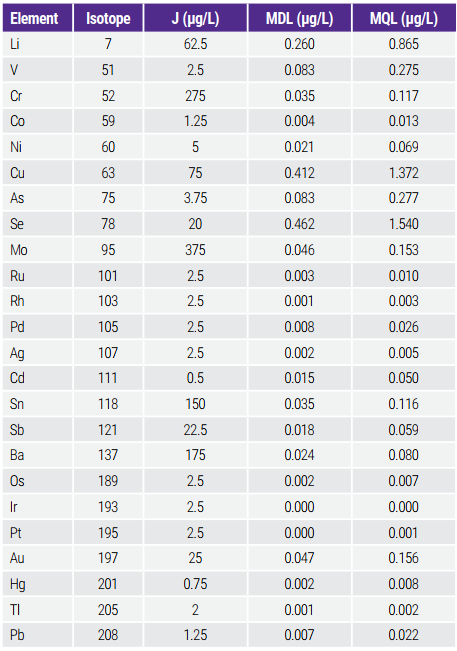
Bảng 5. MDLs and MQLs in Comparison with J
Tính phát hiện (Detectability)
Trong thử nghiệm này, các nồng độ trung bình của các mẫu được thêm tạp chất ở mức 1.0J và 0.8J, đo trong ba lần lặp lại, được so sánh. Theo tiêu chí chấp nhận, nồng độ trung bình (n=3) của các mẫu được thêm tạp chất ở mức 1.0J phải nằm trong phạm vi ± 15% của dung dịch chuẩn 1J. Các mẫu ở mức 0.8J phải cung cấp cường độ tín hiệu hoặc giá trị thấp hơn so với dung dịch chuẩn 1J. Kết quả được trình bày trong Bảng 6 cho thấy các tiêu chí này đã được đáp ứng/vượt qua.
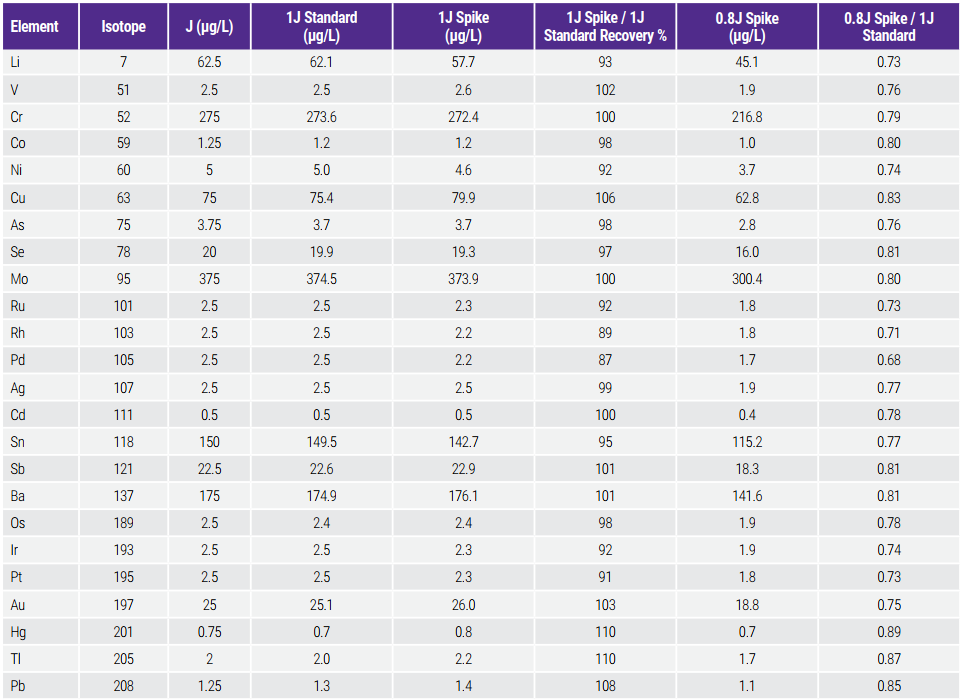
Bảng 6. Detectability Test Results
Độ phù hợp của hệ thống (System Suitability – Stability/Drift)
Thử nghiệm này yêu cầu so sánh kết quả thu được từ dung dịch chuẩn 1.5J trước và sau khi phân tích một loạt mẫu. Tiêu chí chấp nhận yêu cầu độ lệch không quá 20% đối với mỗi nguyên tố mục tiêu. Bảng 7 cho thấy kết quả đối với dung dịch chuẩn 1.5J được đo trước và sau khi phân tích lô 45 mẫu muối (≈2 giờ). Các tiêu chí đã dễ dàng được đáp ứng với độ lệch dưới 6,3%.
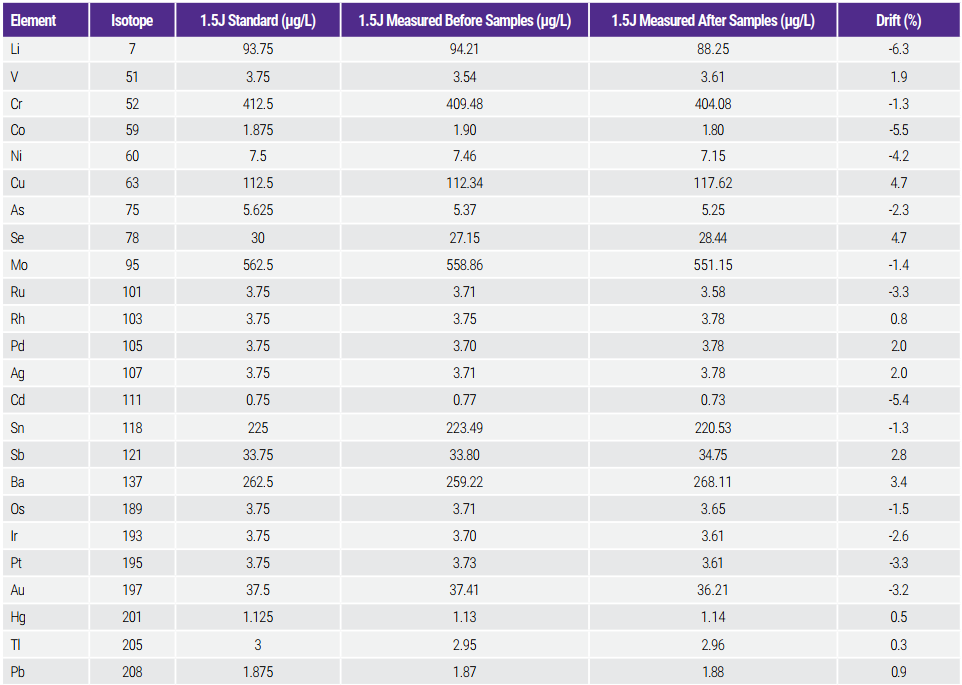
Bảng 7. Stability/Drift Test Results
Độ chính xác (Accuracy)
Hiệu suất thu hồi chất phân tích trên nền mẫu được sử dụng để xác nhận độ chính xác. Theo USP, các tiêu chuẩn phù hợp ở nồng độ từ 0.5J đến 1.5J cũng như các tạp chất tương ứng phải được đo với tiêu chí chấp nhận là tỷ lệ phục hồi tạp chất từ 70% đến 150%. Tuy nhiên, các công ty dược phẩm thường áp dụng các tiêu chí chấp nhận nghiêm ngặt hơn bằng cách đánh giá các tạp chất ở mức thấp hơn để có đánh giá rủi ro tốt hơn. Do đó, tỷ lệ phục hồi tạp chất ở ba mức (0.3J, 1.0J và 1.5J) đã được đo trong thử nghiệm này. Kết quả được trình bày trong Bảng 8. Tỷ lệ phục hồi tạp chất trong khoảng 85% đến 110% đã đạt được cho tất cả các mức, bao gồm cả mức 0.3J. Đối với tất cả các nguyên tố mục tiêu, độ lệch chuẩn tương đối (RSD, n=3) dưới 10% đối với mức 0.3J và dưới 5% đối với mức 1.0J và 1.5J.
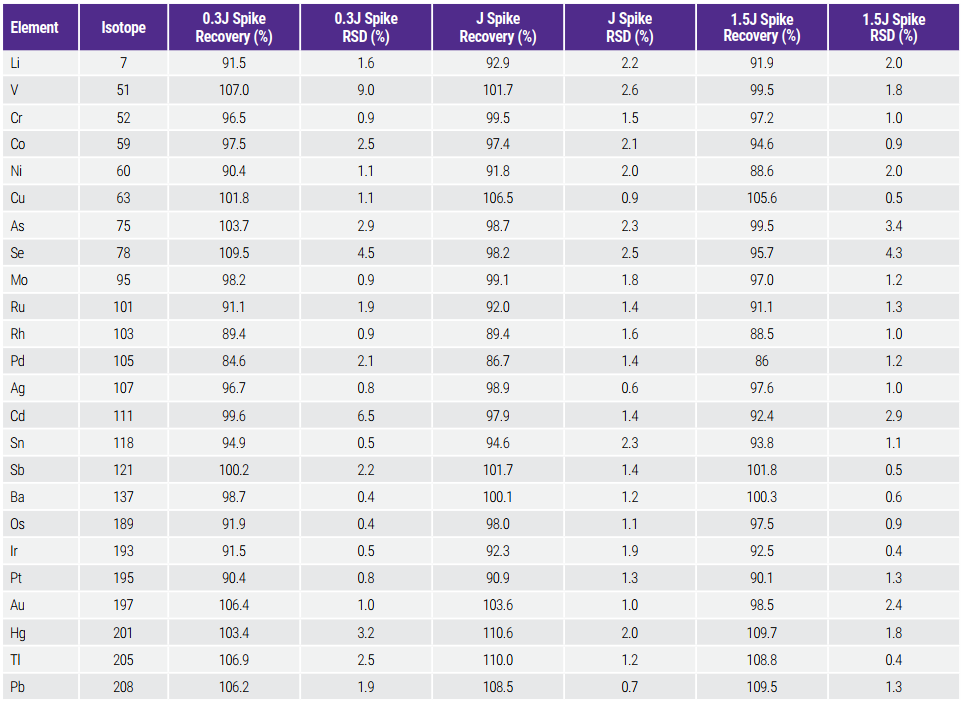
Bảng 8. Accuracy Assessment
Độ chính xác lặp lại và độ chính xác trung gian (Precision/Repeatability and Intermediate Precision)
Trong thử nghiệm độ chính xác lặp lại, RSD của sáu mẫu có tạp chất ở mức 1J (mức mục tiêu) không được quá 20% đối với mỗi nguyên tố mục tiêu. Tiêu chí chấp nhận cho thử nghiệm độ chính xác trung gian là tương tự; tuy nhiên, phân tích sáu mẫu này phải được thực hiện vào các ngày khác nhau, hoặc với các thiết bị khác nhau, hoặc bởi các nhà phân tích khác nhau. Tiêu chí RSD là nhỏ hơn hoặc bằng 25%. Như được hiển thị trong Bảng 9, các RSD là < 6.4% và < 6.6% đối với độ chính xác lặp lại và độ chính xác trung gian, tương ứng, thấp hơn nhiều so với các yêu cầu kỹ thuật.
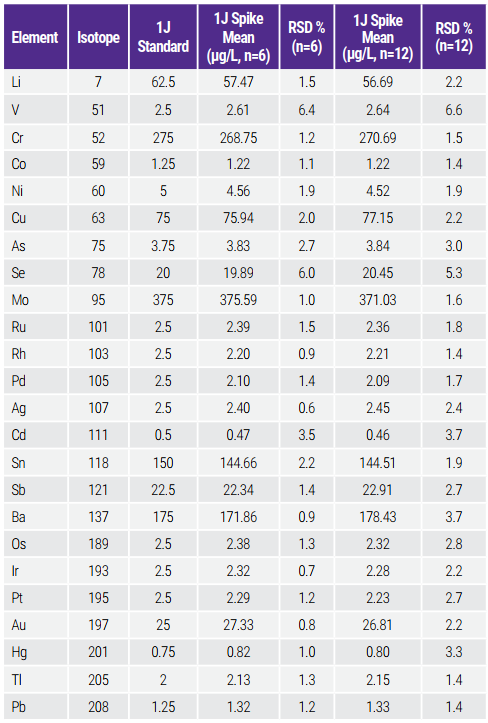
Bảng 9. Precision/Repeatability and Intermediate Precision Tests Results
Kết luận
Nghiên cứu này cho thấy NexION 1100 ICP-MS hoạt động trong chế độ va chạm khí heli (KED) rất phù hợp để phân tích các sản phẩm dược phẩm theo các chương USP và hài hòa với ICH Q3D. Dung dịch muối truyền tĩnh mạch là một trong những sản phẩm dược phẩm thách thức nhất để phân tích do thể tích lớn, tổng lượng chất rắn hòa tan cao (TDS) và các PDE thấp. Tất cả 24 nguyên tố đã được xác định và định lượng bằng cách sử dụng chế độ va chạm khí heli (KED) để loại bỏ các nhiễu đa nguyên tử tiềm năng, và tất cả các yêu cầu xác nhận đã dễ dàng được đáp ứng đối với tính tuyến tính, giới hạn phát hiện (tính phát hiện), độ phù hợp của hệ thống (tính ổn định), độ chính xác và độ chính xác lặp lại và trung gian.
Tài liệu tham khảo
- United States Pharmacopeia General Chapter Elemental Impurities – Limits: USP 40 (First Supplement, 2017).
- United States Pharmacopeia General Chapter Elemental Impurities – Procedures: USP 38 (Second Supplement, 2015).
- ICH guideline Q3D (R2) on Elemental Impurities, Step 5, May 2022.
- USP / and ICH Q3D Toolkit, PerkinElmer, 2015.
- NexION 1100 ICP-MS Interactive Brochure, PerkinElmer, 2024.
- NexION Software Guide, PerkinElmer.
- United States Pharmacopeia General Chapter Plasma Spectrochemistry Method in USP National Formulary (NF).
Vật tư tiêu hao sử dụng
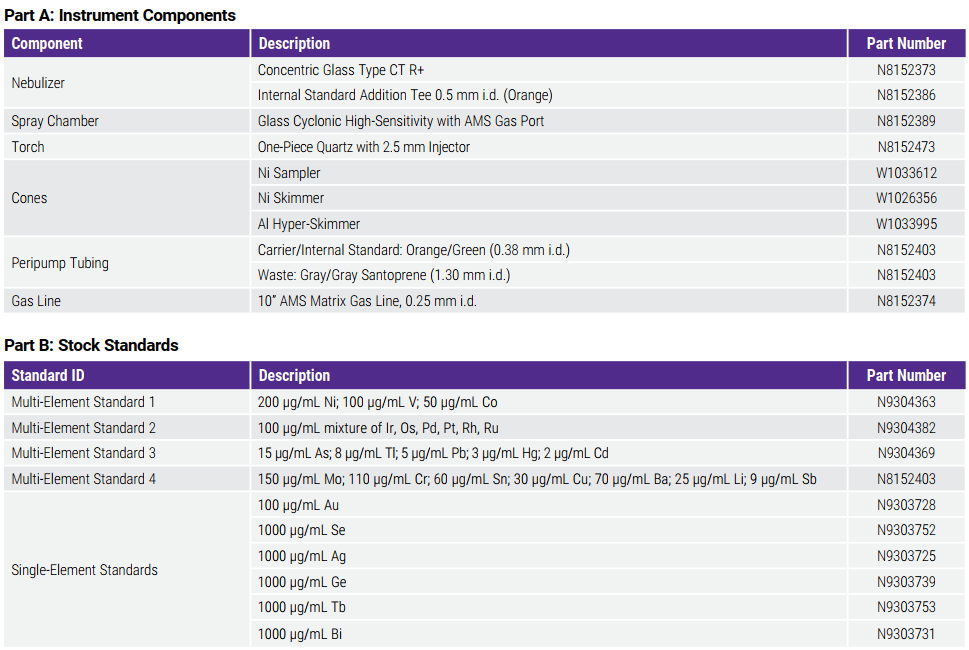
Tài liệu tải về